chemie Stanovení isosbestického bodu bromkresolové zeleně (BKZ) Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Návaznost experimentů
|
|
|
- Gabriela Krausová
- před 8 lety
- Počet zobrazení:
Transkript
1 Stanovení isosbestického bodu bromkresolové zeleně (BKZ) pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 20 úloha číslo Cíle Cílem této laboratorní úlohy je stanovení isosbestického bodu acidobazického indikátoru bromkresolová zeleň proměřením absorpčních spekter ve viditelné oblasti roztoku indikátoru v prostředí o různém ph. Podrobnější rozbor cílů Použít odpovídající instrumentální vybavení spektrofotometr AMADEUS. Připravit roztoky kyseliny chlorovodíkové o různých hodnotách ph a roztok acidobazického indikátoru bromkresolová zeleň (BKZ). Připravit roztoky indikátoru BKZ v prostředí o různé hodnotě ph. Změřit absorpční spektra roztoků BKZ v prostředí o různé hodnotě ph. Na základě změřených spekter určit isosbestický bod. Zařazení do výuky Laboratorní úlohu je vhodné zařadit v rámci učiva středoškolské chemie, organická chemie (barevnost látek), v kapitole praktické využití chemie barviva, případně při rozšířené výuce analytická chemie. Časová náročnost Dvě vyučovací hodiny, tj min. Zadání úlohy Stanovte hodnotu isosbestického bodu acidobazického indikátoru bromkresolová zeleň BKZ) proměřením absorpčních spekter ve viditelné oblasti roztoku indikátoru v prostředí o různém ph. Pro urychlení úlohy je praktické mít dopředu připravený roztok bromkresolové zeleně, eventuelně i roztoky HCl, tj. roztoky o různé hodnotě ph. Návaznost experimentů Experiment může být navazující na úlohu Měření spekter barviv (přírodních nebo syntetických). Na tuto úlohu může navazovat úloha Stanovení disociační konstanty acidobazického indikátoru. Mezipředmětové vztahy fyzika optika Pomůcky počítač s USB portem; diode-array spektrofotometr AMADEUS; sada plastových kyvet (PS); software Data- Studio nebo zařízení SPARK; 0,001 M roztok HCl ; 0,1% roztok bromkresolové zeleně (BKZ) 100 ml; destilovaná voda 100 ml; dělené pipety 10 ml, 5 ml a 1 ml případně automatická pipeta; pipetovací nástavec; odměrné baňky (5 ks); odpadní kádinka 250 ml (1 ks); popisovač odměrných baněk (lihový fix); pracovní návod; pracovní list; ochranné pracovní pomůcky Experimentem k poznání 239
2 20 Stanovení isosbestického bodu bromkresolové zeleně (BKZ) chemie Teoretický úvod Při kontaktu látky s elektromagnetickým zářením, tedy světlem, může dojít k pohlcení (absorpci) části světla, tj. určitých energií resp. vlnových délek světla. Tato energie je v látce využita na exitaci elektronů na vyšší energetické hladiny. Energetický rozdíl těchto hladin odpovídá absorbované energii světla podle tzv. Planckova zákona. c E = h = h ( 1 ) 0 VZOREK Obr. 1: Průchod záření vzorkem E energie absorbovaného záření, resp. energetický rozdíl hladin h Planckova konstanta, h = 6, ³⁴ J s ν frekvence světla c rychlost světla (ve vakuu c = m s ¹) λ vlnová délka Ze vztahu (1) vyplývá, že čím je vyšší frekvence pohlceného záření, tím je jeho energie vyšší, tedy čím má světlo menší vlnovou délku, tím je energeticky bohatší. Při absorpci světla dochází k poklesu zářivého toku, jak naznačuje obrázek 1. Podíl zářivého toku (po průchodu látkou) vůči původnímu ₀ (před průchodem látkou) nazýváme transmitance (propustnost) a dosahuje hodnot 0 1, resp %. T = ( 2 ) ₀ A Pokud provedeme záporný logaritmus této veličiny, získáme veličinu absorbance, která charakterizuje velikost absorpce. A = log T = log ₀ ( 3 ) Tato veličina je závislá na koncentraci látky c, délce absorbující vrstvy l a na molárním absorpčním koeficientu ε, který je mj. závislý na vlnové délce. Frekvenci, resp. vlnovou délku záření, při níž nabývá ε maximálních hodnot, pak nazýváme absorpčním maximem λ[nm] Obr. 2: Absorpční spektrum A = ε l c ( 4 ) Závislost absorbance na vlnové délce potom nazýváme absorpční spektrum. Acidobazické indikátory jsou látky, které mění svou barvu v závislosti na ph prostředí, tato změna souvisí se změnou jejich struktury, a tedy se změnou jejich spektra. Jak můžeme vidět na obrázku 3. Jednotlivá spektra indikátoru methyloranž se mění v závislosti na ph prostředí. Absorpční maximum odpovídající vyšší vlnové délce má maximální hodnotu v silně kyselé oblasti, zatímco absorpční maximum odpovídající nižší vlnové délce odpovídá nejméně kyselému prostředí. Všechna spektra se protínají v bodě, který je charakteristický pro daný acidobazický indikátor. Tento bod se nazývá isosbestický. 240 Gymnázium Polička
3 chemie Stanovení isosbestického bodu bromkresolové zeleně (BKZ) úloha číslo 20 A 1 1 ph 2,2 2 ph 3,8 3 ph 5, λ[nm] Obr. 3: Absorpční spektra indikátoru methyloranž v závislosti na ph prostředí Motivace Ptáme se studentů, co pozorují, když přidají do ovocného čaje nebo ovocné šťávy citrón (pozorují barevnou změnu probarvení). Vedeme diskusi, čím je uvedená skutečnost způsobena a zda by se toho dalo nějakým způsobem využít. Můžeme volně navázat na syntetické acidobazické indikátory (methyloranž, fenolftalein) a nechat studenty uvažovat nad důvodem barevné změny všech uvedených látek (tj. změna struktury). Bezpečnost práce Pracujte pečlivě a v souladu s pracovním návodem. V laboratoři používejte ochranné brýle, plášť a případně další pomůcky v souladu se správnou laboratorní praxí. K pipetování roztoku kyseliny chlorovodíkové používejte raději pipetovací nástavec. Příprava úlohy Doporučujeme, aby si studenti nejprve prostudovali teoretickou část a doplnili slovníček pojmů (možno zadat i jako domácí úkol). Ověřte, že studenti přípravnou část úlohy opravdu vypracovali. Postup práce Nastavení HW a SW Propojte řídicí jednotku AMADEUS s počítačem nebo se zařízením SPARK pomocí USB kabelu. Jeden konec světelného vodiče připojte k řídicí jednotce a druhý konec připojte ke spektrofotometru. Dále připojte ke spektrofotometru zdroj el. energie tak, jak je naznačeno na obrázku 4 na následující straně. Spusťte program SPARKVUE nebo zařízení SPARK. Klikněte na tlačítko SESTAVT a zvolte VLNOVÁ DÉLKA a ABSORBANCE (o. d.) a klikněte na ikonu grafu. Poté klikněte na ikonu NÁSTROJE EXPERMENTU (vpravo dole), zvolte nabídku KONFGURACE SENZORŮ. Do spektrofotometru vložte černý hranol s kovovou vymezovací podložkou a zvolte možnost ULOŽT TMAVOU. Poté vložte do spektrofotometru prázdnou kyvetu, popř. kyvetu s destilovanou vodou a zvolte možnost ULOŽT RE- FERENC. Nyní máte spektrofotometr nastavený a připravený k měření. Kyselina chlorovodíková (HCl) způsobuje poleptání. Dráždí dýchací orgány. Při zasažení očí okamžitě důkladně vypláchněte vodou a vyhledejte lékařskou pomoc. Používejte vhodný ochranný oděv, ochranné rukavice a ochranné brýle nebo obličejový štít. V případě úrazu, nebo necítíte-li se dobře, okamžitě vyhledejte lékařskou pomoc. Třída nebezpečnosti C. R S 26-36/37/39-45 Pokud chcete sledovat okamžitou hodnotu absorbance, zvolte v části SESTAVT volbu ABSORBANCE (o. d.) a klikněte na ikonu numerického formátu (čísla). Experimentem k poznání 241
4 20 Stanovení isosbestického bodu bromkresolové zeleně (BKZ) chemie Obr. 4: Zapojení měřicí soustavy Příprava měření Příprava roztoků 1) Do odměrné baňky nalijte asi 10 ml destilované vody. Ze zásobního roztoku 0,001 M HCl odměřte 6, a toto množství převeďte do baňky. Baňku mírně promíchejte, přidejte 1 ml 0,1% roztoku BKZ, doplňte destilovanou vodou po rysku a řádně promíchejte. Tímto způsobem jste připravili roztok o ph = 3,6. Tuto odměrnou baňku označte č. 1, resp. hodnotou ph. 2) Další kalibrační roztoky připravte postupným ředěním tak, jak je naznačeno na obrázku 5. Roztok č. 2 o ph = 4 připravte odměřením 10 ml roztoku č. 1 do odměrné baňky č. 2, kterou doplníte po rysku a řádně promíchejte. Odměřování příslušných objemů provádějte vždy vhodnou pipetou. 2,5 ml 6, 10 ml 8 ml 2,5 ml Při přípravě zásobního roztoku 0,001 M HCl doporučujeme postupovat tak, že si nejprve připravíme 0,1 M HCl (0,88 ml 35% HCl na 100 ml), poté z tohoto roztoku odměříme 1 ml do 100 ml odměrné baňky. Doplněním po rysku získáme zásobní 0,001 M HCl. Způsob postupného ředění je pro tuto úlohu výhodný. Pokud bychom vše ředili ze zásobního roztoku, byly by pipetované objemy příliš malé a dopouštěli bychom se značné chyby (experimentálně ověřeno). Pokud např. při přípravě roztoku č. 1 budete pipetovat 6,3 ml místo 6,, nemá toto zaokrouhlení na hodnotu ph téměř vliv (3,59 místo 3,60). Výjimku při přípravě roztoku č. 4 navrhujeme proto, aby pipetovaný objem bylo rozumné číslo. ph = 3 ph = 3,6 ph = 4 ph = 4,5 ph = 5 ph = 6 0,001 M 100 ml 2, M M Obr. 5: Schéma ředění roztoků o daném ph 3, M M M 3) Podobně si připravte roztok č. 3 o ph = 4,5, roztok č. 4 o ph = 5 (POZOR VÝJMKA PPETOVÁNÍ) a roztok č. 5 o ph = 6. Pro přehlednost je způsob ředění uveden níže: ph = 3,6 (roztok č. 1) Odměřte 6, zásobního roztoku 0,001 M HCl, 1 ml 0,1% roztoku BKZ do baňky a doplňte po rysku. ph = 4,0 (roztok č. 2) Odměřte 10 ml roztoku č. 1, tj. 2,5 10 ⁴ M HCl, 1 ml 0,1% roztoku BKZ do baňky a doplňte po rysku. 242 Gymnázium Polička
5 chemie Stanovení isosbestického bodu bromkresolové zeleně (BKZ) úloha číslo 20 ph = 4,5 (roztok č. 3) Odměřte 8 ml roztoku č. 2, tj. 1,0 10 ⁴ M HCl, 1 ml 0,1% roztoku BKZ do baňky a doplňte po rysku. ph = 5 (roztok č. 4) POZOR VÝJMKA Odměřte 2,5 ml roztoku č. 2, tj. 1,0 10 ⁴ M HCl, 1 ml 0,1% roztoku BKZ do baňky a doplňte po rysku. ph = 6 (roztok č. 5) Odměřte 2,5 ml roztoku č. 4, tj. 1,0 10 ⁴ M HCl, 1 ml 0,1% roztoku BKZ do baňky a doplňte po rysku. 4) Pro kontrolu je vhodné změřit hodnoty ph připravených roztoků. Postup měření ph vč. kalibrace je uveden v úloze ph elektrolytu a hydrolýza solí. Množství roztoku v kyvetě stačí tolik, aby paprsek světla procházel roztokem, tj. aby byla zcela zaplněna užší část kyvety. Není nutné měřit spektra všech 5 roztoků. Postačí změřit spektra u 3 4 z připravených roztoků. Rozpětí ph od 3,6 do 6 (obrázek č. 6) je oblast barevného přechodu BKZ, což můžete studentům demonstrovat. Obr. 6: Připravené roztoky BKZ o ph 3,6 6,0 Vlastní měření a záznam dat 1) Do kyvety nalijte roztok č. 1, kyvetu umístěte společně s kovovou vymezovací podložkou do spektrofotometru tak, aby hladkými protilehlými stěnami procházel světelný paprsek. Klikněte na ikonu tlačítka START (zelená šipka vlevo dole). Okamžitě se objeví celé spektrum, po ustálení spektra klikněte na tlačítko STOP (stejně umístěné). 2) Obsah kyvety vylijte do odpadní kádinky, kyvetu vypláchněte destilovanou vodou a poté následujícím měřeným roztokem. 3) Stejný postup opakujte pro další roztoky. Analýza naměřených dat 1) V panelu nástrojů, v pravé části obrazovky, klikněte na ikonu šipky. Ta se zvýrazní. 2) Poté klikněte do grafu na stanovený isosbestický bod, tj. na průsečík spekter. 3) V horní části obrazovky se zobrazí souřadnice bodu. Vlnová délka určující isosbestický bod odpovídá souřadnici x. 4) Své záznamy uložte pomocí kombinace kláves CTRL+S. Hodnocení výsledků Sestavili a použili studenti měřicí aparaturu správně? Postupovali korektně podle pracovního postupu? Porozuměli studenti uvedené problematice? Vypracovali studenti správně své pracovní listy? Připravili studenti potřebné roztoky správně, tj. dosáhli barevné škály od žluté k modré? Stanovili studenti správně isosbestický bod a ten se shoduje s tabulkovou hodnotou? Syntéza a závěr Poté, co studenti vyplní své pracovní listy, společně shrneme získané poznatky o acidobazických indikátorech a jejich spektrech. Popíšeme souvislost mezi změnou barevnosti indikátoru a jejich strukturou prezentovanou VS spektrem. Experimentem k poznání 243
6 20 Stanovení isosbestického bodu bromkresolové zeleně (BKZ) chemie nformační zdroje index.cfm Gymnázium Polička
chemie chemické reakce Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Zadání úlohy Návaznost experimentů Mezipředmětové vztahy
 Teplo chemické reakce pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 03 úloha číslo Cíle Cílem této laboratorní úlohy je stanovení hodnoty tepla chemické reakce rozkladu
Teplo chemické reakce pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 03 úloha číslo Cíle Cílem této laboratorní úlohy je stanovení hodnoty tepla chemické reakce rozkladu
chemie Měření ph elektrolytů, hydrolýza solí Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Zadání úlohy Návaznost experimentů
 Měření ph elektrolytů, hydrolýza solí pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 07 úloha číslo Cíle Cílem tohoto laboratorního cvičení je měření ph silných a slabých
Měření ph elektrolytů, hydrolýza solí pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 07 úloha číslo Cíle Cílem tohoto laboratorního cvičení je měření ph silných a slabých
chemie Konduktometrická titrace Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Zadání úlohy Návaznost experimentů
 pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada Konduktometrická titrace chemie 08 úloha číslo Cíle Provést titrační stanovení koncentrace kyseliny chlorovodíkové ve vzorku technické
pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada Konduktometrická titrace chemie 08 úloha číslo Cíle Provést titrační stanovení koncentrace kyseliny chlorovodíkové ve vzorku technické
chemie Rychlost chemické reakce Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Návaznost experimentů Zadání úlohy
 Rychlost chemické reakce pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 05 úloha číslo Cíle Cílem této úlohy je sledování rychlosti chemické reakce thiosíranu sodného se
Rychlost chemické reakce pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 05 úloha číslo Cíle Cílem této úlohy je sledování rychlosti chemické reakce thiosíranu sodného se
chemie Stanovení částečné přechodné tvrdosti vody Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Zadání úlohy Návaznost experimentů
 Stanovení částečné přechodné tvrdosti vody pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 13 úloha číslo Cíle Cílem tohoto laboratorního cvičení je stanovení částečné přechodné
Stanovení částečné přechodné tvrdosti vody pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 13 úloha číslo Cíle Cílem tohoto laboratorního cvičení je stanovení částečné přechodné
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 2 (30 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Adsorpce barviva na aktivním uhlí
 Adsorpce barviva na aktivním uhlí TEORIE ABSORBANCE Prochází-li světelný tok monochromatických paprsků o intenzitě I 0 určitým prostředím dojde k pohlcení jisté části záření a intenzita záření se sníží
Adsorpce barviva na aktivním uhlí TEORIE ABSORBANCE Prochází-li světelný tok monochromatických paprsků o intenzitě I 0 určitým prostředím dojde k pohlcení jisté části záření a intenzita záření se sníží
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE)
 NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
pracovní list studenta Komplexní sloučeniny Stanovení koncentrace železnaté soli Aleš Mareček
 Výstup RVP: Klíčová slova: Komplexní sloučeniny Aleš Mareček žák se seznámí s moderní měřicí technikou a propojí poznatky z oblasti fyziky s metodami chemické analýzy, dále si rozšíří vědomosti z oblasti
Výstup RVP: Klíčová slova: Komplexní sloučeniny Aleš Mareček žák se seznámí s moderní měřicí technikou a propojí poznatky z oblasti fyziky s metodami chemické analýzy, dále si rozšíří vědomosti z oblasti
pracovní list studenta Analytická chemie Barevnost chemických látek Aleš Mareček
 Výstup RVP: Klíčová slova: Analytická chemie Aleš Mareček žák se na základě vlastního pozorování seznámí s příčinami barevnosti chemických sloučenin; v průběhu práce získá základní informace o moderních
Výstup RVP: Klíčová slova: Analytická chemie Aleš Mareček žák se na základě vlastního pozorování seznámí s příčinami barevnosti chemických sloučenin; v průběhu práce získá základní informace o moderních
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE)
 SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
chemie Chemické hodiny Cíle Zařazení do výuky Podrobnější rozbor cílů Zadání úlohy Časová náročnost Pomůcky Návaznost experimentů
 Chemické hodiny pracovní návod s metodickým komentářem pro učitele připravil T. Feltl chemie 04 úloha číslo Cíle Demonstrace oscilačních reakcí jako úvod k chemické kinetice. Podrobnější rozbor cílů Seznámení
Chemické hodiny pracovní návod s metodickým komentářem pro učitele připravil T. Feltl chemie 04 úloha číslo Cíle Demonstrace oscilačních reakcí jako úvod k chemické kinetice. Podrobnější rozbor cílů Seznámení
Měření koncentrace roztoku absorpčním spektrofotometrem
 Měření koncentrace roztoku absorpčním spektrofotometrem Teoretický úvod Absorpční spektrofotometrie je metoda stanovení koncentrace disperzního podílu analytické disperze, založená na měření absorpce světla.
Měření koncentrace roztoku absorpčním spektrofotometrem Teoretický úvod Absorpční spektrofotometrie je metoda stanovení koncentrace disperzního podílu analytické disperze, založená na měření absorpce světla.
Oborový workshop pro SŠ CHEMIE
 PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro SŠ CHEMIE
PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro SŠ CHEMIE
pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů
 Výstup RVP: Klíčová slova: pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů Aleš Mareček žák se seznámí s moderními metodami kvantitativní analýzy (práce propojuje
Výstup RVP: Klíčová slova: pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů Aleš Mareček žák se seznámí s moderními metodami kvantitativní analýzy (práce propojuje
Změna teploty varu roztoku demonstrační pokus VY_52_Inovace_222 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8
 Změna teploty varu roztoku demonstrační pokus VY_52_Inovace_222 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8 Kapitola: Směsi Téma: Roztoky Cíl: Sledovat zvyšování teploty varu
Změna teploty varu roztoku demonstrační pokus VY_52_Inovace_222 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8 Kapitola: Směsi Téma: Roztoky Cíl: Sledovat zvyšování teploty varu
fenanthrolinem Příprava
 1 ÚLOHA 9: Spektrofotometrické fenanthrolinem studium komplexu Fe(II) s 1,10- Příprava 2. 3. 4. 5. 6. Zopakujte si základní pojmy z optiky - elektromagnetické záření a jeho šíření absorbujícím prostředím,
1 ÚLOHA 9: Spektrofotometrické fenanthrolinem studium komplexu Fe(II) s 1,10- Příprava 2. 3. 4. 5. 6. Zopakujte si základní pojmy z optiky - elektromagnetické záření a jeho šíření absorbujícím prostředím,
Práce se spektrometrem SpectroVis Plus Vernier
 informace pro učitele Práce se spektrometrem SpectroVis Plus Vernier Aleš Mareček Kvinta úloha Měřené veličiny Přístroj SpectroVis Plus umožní studovat viditelnou část spektra a část blízké infračervené
informace pro učitele Práce se spektrometrem SpectroVis Plus Vernier Aleš Mareček Kvinta úloha Měřené veličiny Přístroj SpectroVis Plus umožní studovat viditelnou část spektra a část blízké infračervené
Pracovní návod 1/7 www.expoz.cz
 Pracovní návod 1/7 www.expoz.cz Chemie úloha č. 14 Kolik železa spolykáme Autor: Tomáš Feltl Cíle Seznámení se s teoretickým a praktickým základem spektrofotometrických metod na příkladu stanovení koncentrace
Pracovní návod 1/7 www.expoz.cz Chemie úloha č. 14 Kolik železa spolykáme Autor: Tomáš Feltl Cíle Seznámení se s teoretickým a praktickým základem spektrofotometrických metod na příkladu stanovení koncentrace
Neutralizace, měření senzorem ph Vernier Laboratorní práce
 Neutralizace, měření senzorem ph Vernier Laboratorní práce VY_52_INOVACE_209 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Neutralizace, měření senzorem ph Vernier Laboratorní
Neutralizace, měření senzorem ph Vernier Laboratorní práce VY_52_INOVACE_209 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Neutralizace, měření senzorem ph Vernier Laboratorní
Molekulová spektroskopie 1. Chemická vazba, UV/VIS
 Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
chemie Stanovení obsahu vápenatých iontů v minerální vodě Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Zadání úlohy
 Stanovení obsahu vápenatých iontů v minerální vodě pracovní návod s metodickým komentářem pro učitele připravil T. Feltl chemie 12 úloha číslo Cíle Stanovení koncentrace vápenatých iontů v minerální vodě
Stanovení obsahu vápenatých iontů v minerální vodě pracovní návod s metodickým komentářem pro učitele připravil T. Feltl chemie 12 úloha číslo Cíle Stanovení koncentrace vápenatých iontů v minerální vodě
Kurz 1 Úvod k biochemickému praktiku
 Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Zařazení do výuky Experiment je vhodné zařadit v rámci učiva chemie v 8. třídě (kyseliny, zásady, ph roztoků).
 Název: Dýchání do vody Úvod Někdy je celkem jednoduché si v chemické laboratoři nebo dokonce i doma připravit kyselinu. Pokud máte kádinku, popř. skleničku, a brčko, tak neváhejte a můžete to zkusit hned!
Název: Dýchání do vody Úvod Někdy je celkem jednoduché si v chemické laboratoři nebo dokonce i doma připravit kyselinu. Pokud máte kádinku, popř. skleničku, a brčko, tak neváhejte a můžete to zkusit hned!
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I
 1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
Kyseliny a zásady měření ph indikátory a senzorem ph Vernier Laboratorní práce
 Kyseliny a zásady měření ph indikátory a senzorem ph Vernier Laboratorní práce VY_52_INOVACE_204 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Kyseliny a zásady měření ph indikátory
Kyseliny a zásady měření ph indikátory a senzorem ph Vernier Laboratorní práce VY_52_INOVACE_204 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Kyseliny a zásady měření ph indikátory
Stanovení koncentrace složky v roztoku vodivostním měřením
 Laboratorní úloha B/2 Stanovení koncentrace složky v roztoku vodivostním měřením Úkol: A. Stanovte vodivostním měřením koncentraci HCl v dodaném vzorku roztoku. Zjistěte vodivostním měřením body konduktometrické
Laboratorní úloha B/2 Stanovení koncentrace složky v roztoku vodivostním měřením Úkol: A. Stanovte vodivostním měřením koncentraci HCl v dodaném vzorku roztoku. Zjistěte vodivostním měřením body konduktometrické
ULTRAFIALOVÁ A VIDITELNÁ SPEKTROMETRIE
 Pracovní úkol 1. Vytvořte kalibrační řadu roztoků pro stanovení orthofosforečnanů (viz část 1), stanovte vhodnou vlnovou délku pro kalibraci a proveďte kalibraci přístroje pro toto stanovení. 2. Na základě
Pracovní úkol 1. Vytvořte kalibrační řadu roztoků pro stanovení orthofosforečnanů (viz část 1), stanovte vhodnou vlnovou délku pro kalibraci a proveďte kalibraci přístroje pro toto stanovení. 2. Na základě
Kapitola: Přírodní látky Téma: Vitamíny. Cíl: Porovnat průběh a rychlost rozpouštění pevných forem vitamínu C v kyselině chlorovodíkové
 Sledování rozpustnosti vitamínu C v žaludeční kyselině demonstrační pokus VY_52_Inovace_244 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8, 9 Kapitola: Přírodní látky Téma: Vitamíny
Sledování rozpustnosti vitamínu C v žaludeční kyselině demonstrační pokus VY_52_Inovace_244 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8, 9 Kapitola: Přírodní látky Téma: Vitamíny
biologie Výstupový test Cíle Zařazení do výuky Podrobnější rozbor cílů Zadání úlohy Časová náročnost Návaznost experimentů Pomůcky
 Výstupový test pracovní návod s metodickým komentářem pro učitele připravila M. Najbertová biologie úloha číslo 03 Cíle Stanovit tělesnou zdatnost výstupovým testem. Podrobnější rozbor cílů Naučit se pracovat
Výstupový test pracovní návod s metodickým komentářem pro učitele připravila M. Najbertová biologie úloha číslo 03 Cíle Stanovit tělesnou zdatnost výstupovým testem. Podrobnější rozbor cílů Naučit se pracovat
Balmerova série. F. Grepl 1, M. Benc 2, J. Stuchlý 3 Gymnázium Havlíčkův Brod 1, Gymnázium Mnichovo Hradiště 2, Gymnázium Šumperk 3
 Balmerova série F. Grepl 1, M. Benc 2, J. Stuchlý 3 Gymnázium Havlíčkův Brod 1, Gymnázium Mnichovo Hradiště 2, Gymnázium Šumperk 3 Grepl.F@seznam.cz Abstrakt: Metodou dělených svazků jsme určili lámavý
Balmerova série F. Grepl 1, M. Benc 2, J. Stuchlý 3 Gymnázium Havlíčkův Brod 1, Gymnázium Mnichovo Hradiště 2, Gymnázium Šumperk 3 Grepl.F@seznam.cz Abstrakt: Metodou dělených svazků jsme určili lámavý
Důkaz kyselin. Metodický list pro učitele. Časový harmonogram. a) doba na přípravu - 10 minut b) doba na provedení 10 minut.
 Důkaz kyselin Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení 10 minut Pomůcky a) chemikálie - kyselina dusičná - kyselina chlorovodíková - kyselina citronová
Důkaz kyselin Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení 10 minut Pomůcky a) chemikálie - kyselina dusičná - kyselina chlorovodíková - kyselina citronová
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
V-A charakteristika polovodičové diody
 FYZIKA V-A charakteristika polovodičové diody Studenti změří napětí na diodě a proud procházející diodou. Z naměřených hodnot sestrojí voltampérovou charakteristiku. Gymnázium Frýdlant, Mládeže 884, příspěvková
FYZIKA V-A charakteristika polovodičové diody Studenti změří napětí na diodě a proud procházející diodou. Z naměřených hodnot sestrojí voltampérovou charakteristiku. Gymnázium Frýdlant, Mládeže 884, příspěvková
Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje.
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU
 FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU návod vznikl jako součást bakalářské práce Martiny Vidrmanové Fluorimetrie s využitím spektrofotometru SpectroVis Plus firmy Vernier (http://is.muni.cz/th/268973/prif_b/bakalarska_prace.pdf)
FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU návod vznikl jako součást bakalářské práce Martiny Vidrmanové Fluorimetrie s využitím spektrofotometru SpectroVis Plus firmy Vernier (http://is.muni.cz/th/268973/prif_b/bakalarska_prace.pdf)
ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ
 ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní
ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní
Spektroskopie v UV-VIS oblasti. UV-VIS spektroskopie. Roztok KMnO 4. pracuje nejčastěji v oblasti 200-800 nm
 Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
Příprava roztoku o dané koncentraci Laboratorní práce
 Příprava o dané koncentraci Laboratorní práce VY_52_INOVACE_197 Vzdělávací oblast: Člověk a příroda Vzdělávací obor:chemie Ročník: 8, 9 Příprava o dané koncentraci Laboratorní práce Jméno Třída..Datum
Příprava o dané koncentraci Laboratorní práce VY_52_INOVACE_197 Vzdělávací oblast: Člověk a příroda Vzdělávací obor:chemie Ročník: 8, 9 Příprava o dané koncentraci Laboratorní práce Jméno Třída..Datum
Chloridová iontově selektivní elektroda
 Chloridová iontově selektivní elektroda Produktové číslo: FU-ENCHL-A018A Chloridy jsou sloučeniny chloru s jiným prvkem, chlor v nich zaujímá podobu iontu Cl-. Jejich nejznámějším zástupcem je chlorid
Chloridová iontově selektivní elektroda Produktové číslo: FU-ENCHL-A018A Chloridy jsou sloučeniny chloru s jiným prvkem, chlor v nich zaujímá podobu iontu Cl-. Jejich nejznámějším zástupcem je chlorid
Derivační spektrofotometrie a rozklad absorpčního spektra
 Derivační spektrofotometrie a rozklad absorpčního spektra Teorie: Derivační spektrofotometrie, využívající derivace absorpční křivky, je obecně používanou metodou pro zvýraznění detailů průběhu záznamu,
Derivační spektrofotometrie a rozklad absorpčního spektra Teorie: Derivační spektrofotometrie, využívající derivace absorpční křivky, je obecně používanou metodou pro zvýraznění detailů průběhu záznamu,
Neutralizace kyseliny zásadou
 Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný
Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný
ÚSTAV ORGANICKÉ TECHNOLOGIE
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
Základy fotometrie, využití v klinické biochemii
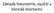 Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace
 Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková
Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková
Název: Pozorování a měření emisních spekter různých zdrojů
 Název: Pozorování a měření emisních spekter různých zdrojů Autor: Doc. RNDr. Milan Rojko, CSc. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: fyzika, chemie Ročník:
Název: Pozorování a měření emisních spekter různých zdrojů Autor: Doc. RNDr. Milan Rojko, CSc. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: fyzika, chemie Ročník:
Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje.
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách
 Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
Název: Acidobazické indikátory
 Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
OBCHOD S KOVOVÝM ŠROTEM (ČÁST 1)
 OBCHOD S KOVOVÝM ŠROTEM (ČÁST 1) Měď je rozšířený kov používaný například do počítačů, jako elektrické kabely, okapy, instalatérské prvky a všemožný spojovací materiál. Po mědi je tedy velká poptávka,
OBCHOD S KOVOVÝM ŠROTEM (ČÁST 1) Měď je rozšířený kov používaný například do počítačů, jako elektrické kabely, okapy, instalatérské prvky a všemožný spojovací materiál. Po mědi je tedy velká poptávka,
Úvod. Náplň práce. Úkoly
 Název práce: Zkouška disoluce pevných lékových forem Vedoucí práce: Doc. Ing. Petr Zámostný, Ph.D. Jméno zástupce: Ing. Jan Patera Umístění práce: S25b Úvod Uvolňování léčiva z tuhých perorálních lékových
Název práce: Zkouška disoluce pevných lékových forem Vedoucí práce: Doc. Ing. Petr Zámostný, Ph.D. Jméno zástupce: Ing. Jan Patera Umístění práce: S25b Úvod Uvolňování léčiva z tuhých perorálních lékových
3) Kvalitativní chemická analýza
 3) Kvalitativní chemická analýza Kvalitativní analýza je součástí analytické chemie a zabývá se zjišťováním, které látky (prvky, ionty, sloučeniny, funkční skupiny atd.) jsou obsaženy ve vzorku. Lze ji
3) Kvalitativní chemická analýza Kvalitativní analýza je součástí analytické chemie a zabývá se zjišťováním, které látky (prvky, ionty, sloučeniny, funkční skupiny atd.) jsou obsaženy ve vzorku. Lze ji
Úloha č. 1 Odměřování objemů, ředění roztoků Strana 1. Úkol 1. Ředění roztoků. Teoretický úvod - viz návod
 Úloha č. 1 Odměřování objemů, ředění roztoků Strana 1 Teoretický úvod Uveďte vzorec pro: výpočet směrodatné odchylky výpočet relativní chyby měření [%] Použitý materiál, pomůcky a přístroje Úkol 1. Ředění
Úloha č. 1 Odměřování objemů, ředění roztoků Strana 1 Teoretický úvod Uveďte vzorec pro: výpočet směrodatné odchylky výpočet relativní chyby měření [%] Použitý materiál, pomůcky a přístroje Úkol 1. Ředění
The acquisition of science competencies using ICT real time experiments COMBLAB. Krásný skleník. K čemu je dobrá spektroskopie?
 Krásný skleník K čemu je dobrá spektroskopie? V časopise Zahrádkář se v dopisech čtenářů objevil tento problém: Pan Sklenička se rozhodl postavit na zahradě nový skleník. Bylo to na popud jeho manželky,
Krásný skleník K čemu je dobrá spektroskopie? V časopise Zahrádkář se v dopisech čtenářů objevil tento problém: Pan Sklenička se rozhodl postavit na zahradě nový skleník. Bylo to na popud jeho manželky,
53. ročník 2016/2017
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ŘEŠENÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úkoly: 1. Doplněná Tabulka
Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ŘEŠENÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úkoly: 1. Doplněná Tabulka
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 1 (20 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 1 (20 bodů) PRAKTICKÁ ČÁST 20 BODŮ Úloha 1 Stanovení Ni 2+ a Ca 2+ ve směsi konduktometricky
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 1 (20 bodů) PRAKTICKÁ ČÁST 20 BODŮ Úloha 1 Stanovení Ni 2+ a Ca 2+ ve směsi konduktometricky
PRAKTIKUM II. Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK. Název: Elektrická vodivost elektrolytů. stud. skup.
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM II. Úloha č. 26 Název: Elektrická vodivost elektrolytů Pracoval: Lukáš Vejmelka stud. skup. FMUZV 73) dne 12.12.2013 Odevzdal
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM II. Úloha č. 26 Název: Elektrická vodivost elektrolytů Pracoval: Lukáš Vejmelka stud. skup. FMUZV 73) dne 12.12.2013 Odevzdal
Stanovení celkové kyselosti nápojů potenciometrickou titrací
 Stanovení celkové kyselosti nápojů potenciometrickou titrací Princip metody U acidobazických titrací se využívají dva druhy indikace bodu ekvivalence - vizuální a instrumentální. K vizuální indikaci bodu
Stanovení celkové kyselosti nápojů potenciometrickou titrací Princip metody U acidobazických titrací se využívají dva druhy indikace bodu ekvivalence - vizuální a instrumentální. K vizuální indikaci bodu
Inovace výuky chemie. ph a neutralizace. Ch 8/09
 Inovace výuky chemie ph a neutralizace Ch 8/09 Vzdělávací oblast: Vzdělávací obor: Tematický okruh: Cílová skupina: Klíčová slova: Očekávaný výstup: Člověk a příroda Chemie Anorganické sloučeniny 8. ročník
Inovace výuky chemie ph a neutralizace Ch 8/09 Vzdělávací oblast: Vzdělávací obor: Tematický okruh: Cílová skupina: Klíčová slova: Očekávaný výstup: Člověk a příroda Chemie Anorganické sloučeniny 8. ročník
Stanovení obsahu vápenatých iontů v minerální vodě
 Pracovní návod 1/5 www.expoz.cz Chemie úloha č. 12 Stanovení obsahu vápenatých iontů v minerální vodě Cíle Autor: Tomáš Feltl Stanovení koncentrace vápenatých iontů v minerální vodě a porovnání získané
Pracovní návod 1/5 www.expoz.cz Chemie úloha č. 12 Stanovení obsahu vápenatých iontů v minerální vodě Cíle Autor: Tomáš Feltl Stanovení koncentrace vápenatých iontů v minerální vodě a porovnání získané
Důkaz uhličitanu ve vodním kameni
 Důkaz uhličitanu ve vodním kameni Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Metodický list pro učitele Pomůcky a) chemikálie - ocet b) potřeby - varná konvice zanesená
Důkaz uhličitanu ve vodním kameni Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Metodický list pro učitele Pomůcky a) chemikálie - ocet b) potřeby - varná konvice zanesená
Stanovení kritické micelární koncentrace
 Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera
 Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera Princip Jde o klasickou metodu kvantitativní chemické analýzy. Uhličitan vedle hydroxidu se stanoví ve dvou alikvotních podílech zásobního
Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera Princip Jde o klasickou metodu kvantitativní chemické analýzy. Uhličitan vedle hydroxidu se stanoví ve dvou alikvotních podílech zásobního
Návod k laboratornímu cvičení. Vitamíny
 Úkol č. 1: Přítomnost vitaminu C v ovoci a zelenině Návod k laboratornímu cvičení Vitamíny Pomůcky: třecí miska s tloučkem, filtrační kruh, nálevka, filtrační papír, zkumavky, stojan na zkumavky Chemikálie:
Úkol č. 1: Přítomnost vitaminu C v ovoci a zelenině Návod k laboratornímu cvičení Vitamíny Pomůcky: třecí miska s tloučkem, filtrační kruh, nálevka, filtrační papír, zkumavky, stojan na zkumavky Chemikálie:
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vitamíny Vlhkost vzduchu
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vitamíny Vlhkost vzduchu
53. ročník 2016/2017
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ZADÁNÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úvod Univerzální acidobazické
Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ZADÁNÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úvod Univerzální acidobazické
Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph (laboratorní práce) Označení: EU-Inovace-Ch-8-11
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph (laboratorní práce) Označení: EU-Inovace-Ch-8-11
Tip Žáci z jednotlivých pracovních skupin si mohou přinést vzorky půd ze svých zahrádek a určit jejich ph.
 Název: Vlastnosti půd Úvod Proč se nám nedaří vypěstovat pěkné rododendrony? Proč má soused větší jahody? A co ty kanadské borůvky, také Vám nerostou? Tyto a další podobné otázky si zahrádkáři kladou často.
Název: Vlastnosti půd Úvod Proč se nám nedaří vypěstovat pěkné rododendrony? Proč má soused větší jahody? A co ty kanadské borůvky, také Vám nerostou? Tyto a další podobné otázky si zahrádkáři kladou často.
Název: Redoxní titrace - manganometrie
 Název: Redoxní titrace - manganometrie Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník:
Název: Redoxní titrace - manganometrie Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník:
Senzor může být připojen ke všem měřícím rozhraním platformy einstein.
 Optická brána Produktové číslo: FU-ENFTG137 Optická brána měří čas, jak dlouho se vyskytuje mezi jejími dvěma rameny nějaká překážka. Pro optickou bránu je speciálně navržen nástroj Časový průvodce, který
Optická brána Produktové číslo: FU-ENFTG137 Optická brána měří čas, jak dlouho se vyskytuje mezi jejími dvěma rameny nějaká překážka. Pro optickou bránu je speciálně navržen nástroj Časový průvodce, který
Spektrální charakteristiky
 Spektrální charakteristiky Cíl cvičení: Měření spektrálních charakteristik filtrů a zdrojů osvětlení 1 Teoretický úvod Interakcí elektromagnetického vlnění s libovolnou látkou vzniká optický jev, který
Spektrální charakteristiky Cíl cvičení: Měření spektrálních charakteristik filtrů a zdrojů osvětlení 1 Teoretický úvod Interakcí elektromagnetického vlnění s libovolnou látkou vzniká optický jev, který
SPEKTROMETRIE. aneb co jsem se dozvěděla. autor: Zdeňka Baxová
 SPEKTROMETRIE aneb co jsem se dozvěděla autor: Zdeňka Baxová FTIR spektrometrie analytická metoda identifikace látek (organických i anorganických) všech skupenství měříme pohlcení IČ záření (o různé vlnové
SPEKTROMETRIE aneb co jsem se dozvěděla autor: Zdeňka Baxová FTIR spektrometrie analytická metoda identifikace látek (organických i anorganických) všech skupenství měříme pohlcení IČ záření (o různé vlnové
Obsah soli v potravinách Laboratorní práce
 Obsah soli v potravinách Laboratorní práce VY_52_INOVACE_214 Vzdělávací oblast: Člověk a příroda Vzdělávací obor:chemie Ročník: 8, 9 Obsah soli v potravinách Laboratorní práce Jméno Třída..Datum Úkol:
Obsah soli v potravinách Laboratorní práce VY_52_INOVACE_214 Vzdělávací oblast: Člověk a příroda Vzdělávací obor:chemie Ročník: 8, 9 Obsah soli v potravinách Laboratorní práce Jméno Třída..Datum Úkol:
C-1 ELEKTŘINA Z CITRONU
 Experiment C-1 ELEKTŘINA Z CITRONU CÍL EXPERIMENTU Praktické ověření, že z citronu a také jiných potravin standardně dostupných v domácnosti lze sestavit funkční elektrochemické články. Měření napětí elektrochemického
Experiment C-1 ELEKTŘINA Z CITRONU CÍL EXPERIMENTU Praktické ověření, že z citronu a také jiných potravin standardně dostupných v domácnosti lze sestavit funkční elektrochemické články. Měření napětí elektrochemického
Návod k přístroji Aditest AS1 na měření obsahu antioxidantů v mazacích olejích
 Návod k přístroji Aditest AS1 na měření obsahu antioxidantů v mazacích olejích 1. Princip metody 2. Popis přístroje 3. Roztoky a spotřební materiál 4. Příklad stanovení 5. Výsledky měření, výpočty 6. Typy
Návod k přístroji Aditest AS1 na měření obsahu antioxidantů v mazacích olejích 1. Princip metody 2. Popis přístroje 3. Roztoky a spotřební materiál 4. Příklad stanovení 5. Výsledky měření, výpočty 6. Typy
Dovednosti/Schopnosti. - orientuje se v ČL, který vychází z Evropského lékopisu;
 Jednotka učení 4a: Stanovení obsahu Ibuprofenu 1. diferencování pracovního úkolu Handlungswissen Charakteristika pracovní činnosti Pracovní postup 2. HINTERFRAGEN 3. PŘIŘAZENÍ... Sachwissen Charakteristika
Jednotka učení 4a: Stanovení obsahu Ibuprofenu 1. diferencování pracovního úkolu Handlungswissen Charakteristika pracovní činnosti Pracovní postup 2. HINTERFRAGEN 3. PŘIŘAZENÍ... Sachwissen Charakteristika
chemie Stanovení ph vodných roztoků
 chemie Stanovení ph vodných roztoků Během laboratorního cvičení se studenti seznámí s metodou stanovení ph. Ke stanovení použijeme ph-metr, který nám s velkou přesností (na dvě desetinná místa) určí ph.
chemie Stanovení ph vodných roztoků Během laboratorního cvičení se studenti seznámí s metodou stanovení ph. Ke stanovení použijeme ph-metr, který nám s velkou přesností (na dvě desetinná místa) určí ph.
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut Úloha 1 Příprava Mohrovy soli 15 bodů Mezi podvojné soli patří
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut Úloha 1 Příprava Mohrovy soli 15 bodů Mezi podvojné soli patří
Měření odrazu a absorpce světla (experiment)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Označení: EU-Inovace-F-9-08 Předmět: Fyzika Cílová skupina: 9. třída Autor: Mgr. Monika Rambousková Časová dotace: 1
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Označení: EU-Inovace-F-9-08 Předmět: Fyzika Cílová skupina: 9. třída Autor: Mgr. Monika Rambousková Časová dotace: 1
Charlesův zákon (pt závislost)
 Charlesův zákon (pt závislost) V této úloze pomocí čidla tlaku plynu GPS-BTA a teploměru TMP-BTA (nebo čidla Go!Temp) objevíme součást stavové rovnice ideálního plynu Charlesův zákon popisující izochorický
Charlesův zákon (pt závislost) V této úloze pomocí čidla tlaku plynu GPS-BTA a teploměru TMP-BTA (nebo čidla Go!Temp) objevíme součást stavové rovnice ideálního plynu Charlesův zákon popisující izochorický
CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Mgr. Lenka Horutová Student a konkurenceschopnost
 www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
Trojské trumfy. pražským školám BARVY U ŽIVOČICHŮ A ROSTLIN. projekt CZ.2.17/3.1.00/32718 EVROPSKÝ SOCIÁLNÍ FOND
 EVROPSKÝ SOCIÁLNÍ FOND PRAHA & EU INVESTUJEME DO VAŠÍ BUDOUCNOSTI Pracovní Didaktický list balíček č. 7 č. 9 Trojské trumfy pražským školám projekt CZ.2.17/3.1.00/32718 BARVY U ŽIVOČICHŮ A ROSTLIN A B?
EVROPSKÝ SOCIÁLNÍ FOND PRAHA & EU INVESTUJEME DO VAŠÍ BUDOUCNOSTI Pracovní Didaktický list balíček č. 7 č. 9 Trojské trumfy pražským školám projekt CZ.2.17/3.1.00/32718 BARVY U ŽIVOČICHŮ A ROSTLIN A B?
Stanovení izoelektrického bodu kaseinu
 Stanovení izoelektrického bodu kaseinu Shlukování koloidních částic do větších celků makroskopických rozměrů nazýváme koagulací. Ke koagulaci koloidních roztoků bílkovin dochází porušením solvatačního
Stanovení izoelektrického bodu kaseinu Shlukování koloidních částic do větších celků makroskopických rozměrů nazýváme koagulací. Ke koagulaci koloidních roztoků bílkovin dochází porušením solvatačního
UNIVERZITA KARLOVA V PRAZE Přírodovědecká fakulta
 Červené zelí jako acidobazický indikátor Zdroj: http://www.scifun.org/homeexpts/homeexpts.html [34] Didaktický záměr: Objasnění pojmu ph a acidobazický indikátor. Popis: Žáci si připraví roztok acidobazického
Červené zelí jako acidobazický indikátor Zdroj: http://www.scifun.org/homeexpts/homeexpts.html [34] Didaktický záměr: Objasnění pojmu ph a acidobazický indikátor. Popis: Žáci si připraví roztok acidobazického
SPEKTROFOTOMETRICKÉ STABOVENÍ SO 4 VE VODÁCH
 Pracovní úkol 1. Vytvořte 2 kalibrační řady pro stanovení šestimocného SO 4 a to v rozsahu koncentrací 5-40 mg/l (po 5 mg/l). 2. Na základě absorpční křivky SO 4 určete vhodnou vlnovou délku (λ) s maximální
Pracovní úkol 1. Vytvořte 2 kalibrační řady pro stanovení šestimocného SO 4 a to v rozsahu koncentrací 5-40 mg/l (po 5 mg/l). 2. Na základě absorpční křivky SO 4 určete vhodnou vlnovou délku (λ) s maximální
CHEMIE. Pracovní list č. 7 - žákovská verze Téma: ph. Mgr. Lenka Horutová. Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.
 www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Standardizace. Alkalimetrie. autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Standardizace. Alkalimetrie. autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Spektrometrické metody. Reflexní a fotoakustická spektroskopie
 Spektrometrické metody Reflexní a fotoakustická spektroskopie odraz elektromagnetického záření - souvislost absorpce a reflexe Kubelka-Munk funkce fotoakustická spektroskopie Měření odrazivosti elmg záření
Spektrometrické metody Reflexní a fotoakustická spektroskopie odraz elektromagnetického záření - souvislost absorpce a reflexe Kubelka-Munk funkce fotoakustická spektroskopie Měření odrazivosti elmg záření
215.1.3 NÍZKOTEPLOTNÍ VLASTNOSTI PALIV A MAZIV ÚVOD
 215.1.3 NÍZKOTEPLOTNÍ VLASTNOSTI PALIV A MAZIV ÚVOD Pro bezproblémový chod spalovacích zařízení, motorů a dalších strojních zařízení při nízkých teplotách jsou důležité nízkoteplotní vlastnosti používaných
215.1.3 NÍZKOTEPLOTNÍ VLASTNOSTI PALIV A MAZIV ÚVOD Pro bezproblémový chod spalovacích zařízení, motorů a dalších strojních zařízení při nízkých teplotách jsou důležité nízkoteplotní vlastnosti používaných
"Rozvoj vědy a pokrok poznání se stávají stále obtížnější. Na experimentování již nestačí zápalky a sláma." Richard Philips Feynman
 "Rozvoj vědy a pokrok poznání se stávají stále obtížnější. Na experimentování již nestačí zápalky a sláma." Richard Philips Feynman Tato publikace vznikla díky operačnímu programu Vzdělávání pro konkurenceschopnost
"Rozvoj vědy a pokrok poznání se stávají stále obtížnější. Na experimentování již nestačí zápalky a sláma." Richard Philips Feynman Tato publikace vznikla díky operačnímu programu Vzdělávání pro konkurenceschopnost
Půdy vlastnosti II. (laboratorní práce)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Půdy vlastnosti II. (laboratorní práce) Označení: EU-Inovace-Př-9-39 Předmět: přírodopis Cílová skupina: 9. třída Autor:
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Půdy vlastnosti II. (laboratorní práce) Označení: EU-Inovace-Př-9-39 Předmět: přírodopis Cílová skupina: 9. třída Autor:
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Mgr. Filip Smrčka Masarykova univerzita, Brno prof. RNDr. Přemysl
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Mgr. Filip Smrčka Masarykova univerzita, Brno prof. RNDr. Přemysl
MĚŘENÍ ABSORPCE SVĚTLA SPEKOLEM
 MĚŘENÍ ABSORPCE SVĚTLA SPEKOLEM Průchodem světla homogenním prostředím se jeho intenzita zmenšuje podle Lambertova zákona. Klesne-li intenzita monochromatického světla po projití vrstvou tloušťky l z hodnoty
MĚŘENÍ ABSORPCE SVĚTLA SPEKOLEM Průchodem světla homogenním prostředím se jeho intenzita zmenšuje podle Lambertova zákona. Klesne-li intenzita monochromatického světla po projití vrstvou tloušťky l z hodnoty
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA. Kategorie E ŘEŠENÍ
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ŘEŠENÍ ANORGANICKÁ CHEMIE 16 BODŮ Úloha 1 Vlastnosti sloučenin manganu a chromu 8 bodů 1) Elektronová konfigurace:
Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ŘEŠENÍ ANORGANICKÁ CHEMIE 16 BODŮ Úloha 1 Vlastnosti sloučenin manganu a chromu 8 bodů 1) Elektronová konfigurace:
Název: Archimedův zákon. Úvod. Cíle. Teoretická příprava (teoretický úvod)
 Název: Archimedův zákon Úvod Jeden z nejvýznamnějších učenců starověku byl řecký fyzik a matematik Archimédes ze Syrakus. (žil 287 212 př. n. l.) Zkoumal podmínky rovnováhy sil, definoval těžiště, zavedl
Název: Archimedův zákon Úvod Jeden z nejvýznamnějších učenců starověku byl řecký fyzik a matematik Archimédes ze Syrakus. (žil 287 212 př. n. l.) Zkoumal podmínky rovnováhy sil, definoval těžiště, zavedl
Třída..Datum. 5. upravte interval sběhu dat v průběhu měření: Experiment Sběr dat: délka 300 sekund; 1 vzorek/sekundu, 1 sekunda/vzorek.
 Laboratorní práce Sledování teploty varu ethanolu s využitím čidla teploty Vernier VY_52_Inovace_238 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8, 9 Jméno Třída..Datum Úkol: Sledujte
Laboratorní práce Sledování teploty varu ethanolu s využitím čidla teploty Vernier VY_52_Inovace_238 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8, 9 Jméno Třída..Datum Úkol: Sledujte
Hranolový spektrometr
 Hranolový spektrometr a vodíkové spektrum Ú k o l y 1. Okalibrujte hranolový spektro.. Určente vlnové délky spektrálních čar vodíkové výbojky. 3. Určente kvantové elektronové přechody v atomu vodíku. 4.
Hranolový spektrometr a vodíkové spektrum Ú k o l y 1. Okalibrujte hranolový spektro.. Určente vlnové délky spektrálních čar vodíkové výbojky. 3. Určente kvantové elektronové přechody v atomu vodíku. 4.
